Tiêu chuẩn nào để đánh giá chất lượng xét nghiệm mà các bác sĩ và bệnh nhân nhận được? Chuẩn Công nhận chất lượng CAP là một trong tiêu chuẩn quan trọng được đánh giá cao trên toàn thế giới, giúp các bác sĩ, bệnh nhân lựa chọn phòng xét nghiệm chất lượng cho mình. Ngày 16/6/2025, Xét nghiệm Genome đã đạt công nhận chất lượng CAP cho cả 3 nhóm với 9 xét nghiệm: 𝗣𝗚𝗧 (PGT-A, PGT-A nhanh, PGT-SR;); 𝗡𝗜𝗣𝗧 (E-NIPT 3, E-NIPT 7, E-NIPT 23, E-NIPT 23 Plus, E-NIPT Twin); 𝗡𝗚𝗦 𝗦𝗼𝗹𝗶𝗱 𝗧𝘂𝗺𝗼𝗿 (Cancernext Tissue 1 – 22 gen với hơn 1.800 biến thể).
| Mời Qúy vị cùng Genome tìm hiểu các thông tin: 1. Chuẩn CAP có ý nghĩa gì với bác sĩ và bệnh nhân —> 2. Hành trình Genome đạt chuẩn CAP —> 3. Thông tin về các xét nghiệm đạt CAP —> 4. Hỏi – đáp về chuẩn CAP. |
1. Chuẩn CAP có ý nghĩa gì với bác sĩ và bệnh nhân
1.1 Tổ chức CAP
College of American Pathologists (CAP) – Tổ chức hàng đầu về bệnh học và chất lượng phòng xét nghiệm

– Tổ chức lớn nhất thế giới của các bác sĩ bệnh học được chứng nhận.
– Nhà cung cấp hàng đầu các chương trình công nhận chất lượng phòng xét nghiệm và PT/EQA (Ngoại kiểm)
– Phục vụ bệnh nhân, bác sĩ và cộng đồng.
– Thúc đẩy sự xuất sắc trong bệnh học và y học xét nghiệm toàn cầu.
1.2 Tiêu chuẩn CAP
Tiêu chuẩn CAP là hệ thống quy chuẩn do CAP – xây dựng và phát triển, nhằm đảm bảo các phòng xét nghiệm đạt được chất lượng cao nhất về độ chính xác, an toàn và hiệu quả. Bộ tiêu chuẩn này được cập nhật định kỳ bởi các chuyên gia quốc tế, dựa trên tiến bộ khoa học và yêu cầu thực tiễn của ngành xét nghiệm hiện đại.
1.3 Các tiêu chí đánh giá của CAP
Chương trình kiểm định của CAP bao gồm hơn 3.000 tiêu chí đánh giá toàn diện – từ cơ sở vật chất, nhân sự, năng lực chuyên môn, độ chính xác và độ ổn định của quy trình phân tích, đến hệ thống kiểm soát chất lượng và bảo mật dữ liệu bệnh nhân.
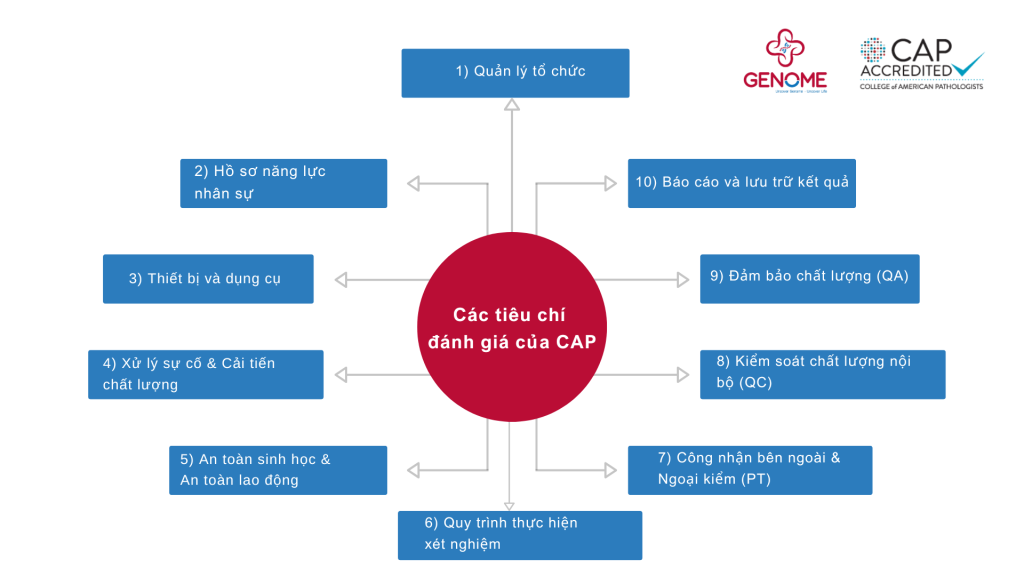
1.4 CAP kiểm chuẩn quốc tế khẳng định chất lượng các phòng xét nghiệm thêm lựa chọn tin cậy cho các bác sĩ và bệnh nhân
Hơn 22.000 phòng xét nghiệm tại hơn 100 quốc gia đã tham gia kiểm chuẩn CAP. Chứng nhận này không chỉ khẳng định chất lượng xét nghiệm mà còn thể hiện cam kết liên tục cải tiến và duy trì môi trường hoạt động chuyên nghiệp, an toàn, hiệu quả.
| Kết quả xét nghiệm chính xác, đáng tin cậy | An toàn cho người bệnh và nhân viên |
| Tối ưu hóa quy trình và thời gian xử lý | Tăng cường minh bạch và truy xuất thông tin |
| Nâng cao uy tín và năng lực cạnh tranh | Hỗ trợ hợp tác quốc tế và công nhận chéo |
2. Hành trình đạt chuẩn CAP của xét nghiệm Genome
2.1. Giai đoạn 1: Tham gia chương trình ngoại kiểm (PT/EQA) được cung cấp bởi chính tổ chức CAP
Một trong những yêu cầu bắt buộc để phòng xét nghiệm có thể nộp đơn xin đăng ký tham gia công nhận bởi CAP là đơn vị phải tham gia và duy trì kết quả đạt trong chương trình Kiểm chuẩn Năng lực (Proficiency Testing – PT) hoặc Đảm bảo Chất lượng Ngoại kiểm (External Quality Assessment – EQA) trong ít nhất 6 tháng liên tục trước khi nộp đơn xin công nhận.
Đây là các chương trình cho phép phòng xét nghiệm đánh giá độ chính xác của quy trình xét nghiệm thông qua việc xử lý các mẫu được mã hóa (blind samples) do CAP hoặc các tổ chức được công nhận cung cấp. Kết quả sẽ được đối chiếu với chuẩn quốc tế và được đánh giá định kỳ.
Genome hoàn thành xuất sắc chương trình Ngoại kiểm Proficiency Testing do CAP tổ chức. Tất cả các đợt đánh giá của Genome đều đạt kết quả 100%, khẳng định chất lượng xét nghiệm ổn định, chính xác và tuân thủ nghiêm ngặt các tiêu chuẩn quốc tế.
2.2. Giai đoạn 2: Chuẩn bị cho quá trình đánh giá, công nhận chất lượng phòng xét nghiệm từ CAP
Bước 1: Đăng Ký Tham Gia Chứng Nhận CAP Trên Hệ Thống
Mọi quy trình đạt chứng nhận CAP bắt đầu bằng việc đăng ký chính thức thông qua website cap.org. Tại đây, phòng xét nghiệm cần lựa chọn loại hình phù hợp với phạm vi hoạt động và loại xét nghiệm đang triển khai, đồng thời cung cấp thông tin pháp lý, quy mô, đội ngũ nhân sự, loại thiết bị và hệ thống quản lý đang áp dụng.
Genome đã đăng ký chương trình đánh giá cho 3 dịch vụ chính gồm: PGT-A, NIPT và sinh thiết mô – tương ứng với các lĩnh vực xét nghiệm di truyền học phân tử và mô bệnh học.
CAP sẽ xem xét tính hợp lệ của đơn đăng ký dựa trên các tiêu chí cơ bản, từ đó khởi tạo hồ sơ cho đơn vị và cung cấp các hướng dẫn chi tiết tiếp theo. Đây là bước quan trọng để chính thức được công nhận là đơn vị đang trong quá trình xét duyệt, đồng thời là cột mốc xác lập cam kết tuân thủ tiêu chuẩn quốc tế.
| Bước 2: Làm việc với đại diện của CAP và hoàn tất hồ sơ đăng ký
Genome phối hợp chặt chẽ với chuyên viên phụ trách của CAP để cung cấp các thông tin hành chính – pháp lý, cũng như mô tả chi tiết về nhân sự, cơ sở vật chất, trang thiết bị, quy trình quản lý và vận hành của phòng xét nghiệm. |
Bước 3: Nhận Bộ Tài Liệu Hướng Dẫn (Welcome Kit) và Truy Cập e-Lab Solutions Suite
Ngay sau khi hồ sơ đăng ký được chấp nhận và chương trình ngoại kiểm được xác minh, CAP sẽ gửi cho phòng xét nghiệm một bộ tài liệu chào mừng (Welcome Kit), bao gồm: Hướng dẫn triển khai hệ thống quản lý chất lượng theo tiêu chuẩn CAP; Quy trình đánh giá và kiểm tra từng mục tiêu kỹ thuật; Mẫu hồ sơ minh chứng; Danh sách các tài liệu bắt buộc
Bước 4: Triển Khai Tự Đánh Giá Theo Danh Mục Tiêu Chuẩn
Sau khi đã nhận được hệ thống tài liệu và hướng dẫn từ CAP, phòng xét nghiệm cần tiến hành đánh giá nội bộ theo bộ tiêu chí kiểm tra do CAP phát hành. Các hạng mục này được chia thành từng nhóm như: Quản lý chất lượng tổng thể; Hiệu chuẩn và bảo trì thiết bị; Quy trình kỹ thuật chuyên môn (ví dụ: xét nghiệm gen di truyền, xét nghiệm ung thư khối u đặc…); Quản lý nhân sự và đào tạo; An toàn sinh học và xử lý chất thải
Mỗi hạng mục sẽ được đánh giá về mức độ tuân thủ, tài liệu chứng minh đi kèm, khả năng truy xuất hồ sơ, cũng như năng lực thực thi tại chỗ.
| Bước 5: Gửi Hồ Sơ Hoàn Chỉnh và Chờ CAP Đánh Giá Sơ Bộ
Sau khi hoàn thiện việc tự đánh giá, đơn vị cần tổng hợp tất cả các minh chứng, biểu mẫu, quy trình và gửi lên hệ thống của CAP. Trong giai đoạn này, các chuyên gia của CAP sẽ tiến hành đánh giá sơ bộ (pre-inspection review), xem xét tính đầy đủ và logic của hệ thống tài liệu. Nếu hồ sơ đạt yêu cầu, đơn vị sẽ chính thức được lên lịch kiểm tra tại chỗ (on-site inspection). |
2.3. Genome đạt Certificate of Participation vào tháng 3/2025
Genome đã đạt bước tiến quan trọng trên hành trình đạt Chứng nhận tiêu chuẩn chất lượng Phòng xét nghiệm CAP Accreditation, với dấu mốc đầu tiên là hoàn thành và đạt chứng nhận tham gia chương trình ngoại kiểm (Proficiency Testing – PT) do CAP cung cấp.

2.4. Đoàn thanh tra CAP đánh giá trực tiếp tại Genome
Ngày 30/5/2025, Xét nghiệm Genome tiếp đón Đoàn chuyên gia đánh giá đến từ CAP, đến thực hiện công tác đánh giá phòng xét nghiệm. Đoàn Chuyên gia CAP gồm có: TS.BS Parrilla Castellar – Giám đốc Phòng xét nghiệm Y khoa tại Phòng xét nghiệm Iqvia – Trưởng đoàn đánh giá CAP, Dr. Paul TJ Tan- Giám đốc Cấp cao Khối Dịch vụ Xét nghiệm Lâm sàng tại Tập đoàn Medpace Singapore – Thành viên đoàn đánh giá.

Đoàn chuyên gia/ thanh tra CAP đã có một ngày làm việc nghiêm túc với rất nhiều hoạt động đánh giá tiêu chuẩn, thực hiện các công tác kiểm tra chặt chẽ như:
– Phỏng vấn đội ngũ Genome: Từ lãnh đạo công ty, lãnh đạo phòng xét nghiệm, đội ngũ nhân sự. Đánh giá các tiêu chuẩn về trình độ, vai trò và trách nhiệm của những người đứng đầu đến các bộ phận.
– Kiểm tra thực tế trung tâm xét nghiệm (lab tour): Không gian, máy móc, công nghệ, hệ thống, quy trình, thuốc thử, vật tư, hệ thống lưu trữ và xử lý chất thải cơ chế cho người bệnh và nhân viên phòng thí nghiệm…
– Kiểm tra chuyên môn của đơn vị của các phòng ban theo các tiêu chí trong bộ yêu cầu, gặp gỡ trao đổi với từng bộ phận, kiểm tra các hồ sơ giấy tờ chuyên môn của từng bộ phận rất kỹ càng cẩn trọng.
– Đoàn kiểm tra trao đổi thẳng thắn với Genome, thảo luận cụ thể, chi tiết về các hạng mục kiểm tra.
– Đoàn thanh tra đưa ra những kết luận, đánh giá rõ ràng ngay cuối ngày kiểm tra tại Genome.
Kết thúc ngày làm việc đoàn thanh tra đánh giá Genome đạt 100% các chỉ tiêu ở ngay lần đánh giá đầu tiên.
2.5. Genome đạt công nhận chất lượng CAP ngày 16/6/2025
Ngày 16/6/2026, CAP chính thức công nhận Trung tâm Xét nghiệm Genome (Hà Nội, Việt Nam) đạt chuẩn chất lượng tối đa ở 5 tiêu chí cho cả 3 nhóm – 9 xét nghiệm:
– PGT- Phân tích di truyền trước chuyển phôi: PGT-A, PGT-A nhanh, PGT-SR,
– NIPT – Sàng lọc trước sinh không xâm lấn: E-NIPT 3, E-NIPT 7, E-NIPT 23, E-NIPT 23 Plus, E-NIPT Twin,
– NGS Solid Tumor – Xét nghiệm mô trong ung thư: CancerNext Tissue 1 (22 gen với hơn 1.800 biến thể).
| C.A.P – Không chỉ là đích đến mà là điểm khởi đầu cho hành trình phát triển mới của Genome – nơi chất lượng quốc tế không còn là mục tiêu xa vời, mà trở thành giá trị cốt lõi, hiện diện trong mỗi xét nghiệm, mỗi con người, mỗi hành động hằng ngày.
Định hướng tiếp theo: Duy trì văn hóa chất lượng bền vững Mở rộng dịch vụ xét nghiệm di truyền chuyên sâu đạt công nhận CAP Tích cực hợp tác nghiên cứu & công nhận quốc tế |
Bài viết liên quan:
PGT – Xét nghiệm di truyền trước chuyển phôi
E-NIPT – Sàng lọc trước sinh không xâm lấn
CancerNext Tissue – Xét nghiệm mẫu mô ung thư
Mời đọc bài tiếp theo: Các xét nghiệm đạt CAP của Genome và các câu hỏi – đáp về Công nhận CAP